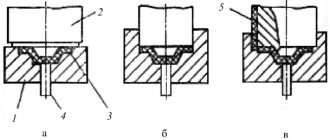
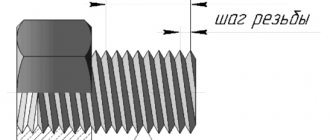
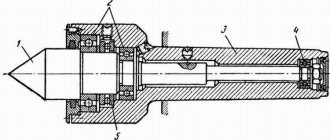
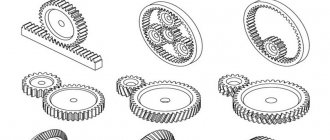
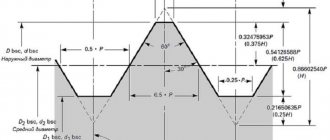
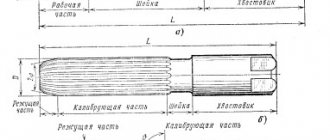
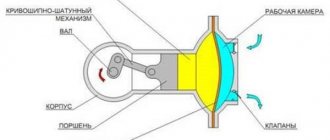
Определение
Как мы знаем, все материальные вещества могут пребывать в трех базовых состояниях: жидком, твердом, и газообразном. Правда есть еще состояние плазмы, которое ученые считают ни много ни мало четвертым состоянием вещества, но наша статья не о плазме. Твердое состояние вещества потому твердое, так как имеет особую кристаллическую структуру, частицы которой находятся в определенном и четко заданном порядке, создавая, таким образом, кристаллическую решетку. Строение кристаллической решетки состоит из повторяющихся одинаковых элементарных ячеек: атомов, молекул, ионов, других элементарных частиц, связанных между собой различными узлами.

Семь типов кристаллических решеток
Есть семь разных кристаллических систем. Они были обнаружены в 1781 году отцом Рене Джаст Хауи. Он случайно заметил, что некоторые камни имеют идеальную форму. После многих лет исследований он разработал свою теорию о структуре кристаллов. В 1848 году Огюст Браве показывает, что может быть только семь типов элементарной кристаллической сетки.
Системы характеризуют различные геометрические формы, которые может иметь кристаллическая сетка.
Каждая из этих систем определяется своими осями: три размерных параметра (длина осей) и три угловых параметра (углы, образованные двумя осями). Условно мы называем abc длинами осей и α β и γ углами, образованными осями. Они размещены в пространстве следующим образом:
Каждая ячейка, представляющая систему, также имеет определенное количество симметрий. Эти симметрии бывают трех типов:
- центральный (отмечен С): точка является центром симметрии сетки;
- плоскости (отмечено P): плоскость является плоскостью симметрии сетки;
- осевой (О): поворот на определенный угол вокруг оси симметрии возвращает сетку в положение, идентичное исходному.
Эти симметрии имеют четыре порядка:
- двоичные ( обозначено L 2 ): вращение на 180 ° (π рад)
- троичное (обозначено L 3 ): вращение на 120 ° (2π/3 рад)
- четвертичное (отмечено L 4 ): Вращение на 90 ° (π/2 рад.)
- гексагональное (отмечено L 6 ): вращение на 60 ° (π/3 рад.)
Кубическая (или изометрическая) решетка
| a = b = c: три оси имеют одинаковую длину α = β = γ= 90 °: три угла равны и прямые Симметрии: C, 3 L 4 , 4 L 3, 6L 2, 9 P Базовый элемент — это куб. |
Квадратичная (или тетрагональная) решетка
| a = b ≠ c: две оси имеют одинаковую длину, а третья ось различается. α = β = γ= 90 °: три угла равны и прямые Симметрии: C, L 4 , 4L2, 5 P Основным элементом является правая призма с квадратным основанием. |
Орторомбическая кристаллическая решетка
| a ≠ b ≠ c: три оси имеют разную длину α = β = γ= 90 °: три угла равны и прямые Симметрии: C, 3 L 2, 3 P Основной элемент — прямоугольный параллелепипед. |
Моноклинная решетка
| a≠b≠c : три оси имеют неравную длину. β = γ= 90 °≠α: два угла равны и прямые. Симметрии: C, L 2 , P Основным элементом является наклонная призма, в основании которой ромб. |
Триклинная решетка
| a≠b≠c: три оси имеют неравную длину. α≠β ≠ γ≠ 90 °: три угла разные. Симметрии: C, L 2 , P Основной элемент — это параллелепипед с основанием ромб. |
Ромбоэдрическая решетка
| a = b = c: три оси имеют одинаковую длину α = β = γ≠ 90 °: три угла равны и прямые Симметрии: C, L 3 , 3 L 2 , P Основным элементом является параллелепипед все плоскости которого — ромбы. |
Виды решеток
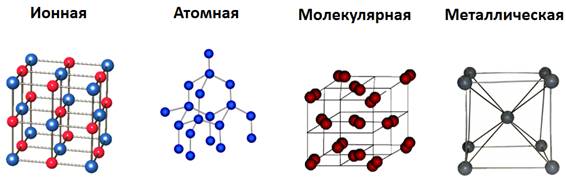
В зависимости от частиц кристаллической решетки существует четырнадцать типов оной, приведем наиболее популярные из них:
Металлическаякристаллическая решетка.
Далее более подробно опишем все типы кристаллической решетки.

Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав – строение – свойства – применение.
Читать также: Сварка ацетиленом и кислородом оборудование
Сведения о кристаллическом строении металлов очень четко иллюстрирует эту зависимость и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.

Содержание:
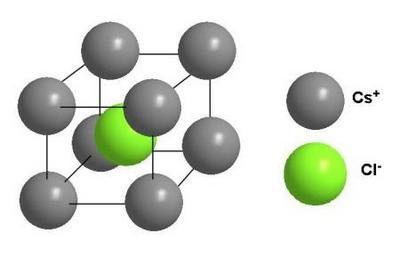
Ионная решетка
Главной особенностью строения кристаллической решетки ионов являются противоположные электрические заряды, собственно, ионов, вследствие чего образуется электромагнитное поле, определяющее свойства веществ, имеющих ионную кристаллическую решетку. А это тугоплавкость, твердость, плотность и возможность проводить электрический ток. Характерным примером ионной кристаллической решетки может быть поваренная соль.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
Рис. 3. Кристаллические ячейки составляют решётку.
Атомная решетка
Вещества с атомной кристаллической решеткой, как правило, имеют в своих узлах, состоящих собственно из атомов сильные ковалентные связи. Ковалентная связь происходит, когда два одинаковых атома делятся друг с другом по-братски электронами, образуя, таким образом, общую пару электронов для соседних атомов. Из-за этого ковалентные связи сильно и равномерно связывают атомы в строгом порядке – пожалуй, это самая характерная черта строения атомной кристаллической решетки. Химические элементы с подобными связями могут похвастаться своей твердостью, высокой температурой плавления. Атомную кристаллическую решетку имеют такие химические элементы как алмаз, кремний, германий, бор.
Молекулярная кристаллическая решётка
В узлах этой структуры находятся молекулы, которые плотно упакованы между собой. Для таких веществ характерна ковалентная полярная и неполярная связь. Интересно, что независимо от ковалентной связи, между частицами образуете очень слабое притяжение (из-за слабых ван-дер-вальсовых сил). Именно поэтому такие вещества очень хрупкие, обладают низкой температурой кипения и плавления, а также они летучие. К таким веществам относятся: вода, органические вещества (сахар, нафталин), оксид углерода (IV), сероводород, благородные газы, двух– (водород, кислород, хлор, азот, йод), трёх- (озон), четырёх- (фосфор), восьмиатомные (сера) вещества и так далее.
Одна из отличительных черт — это то, что структурная и пространственная модель сохраняется во всех фазах (как в твёрдых, так в жидких и газообразных).
Металлическая решетка
Тип связи металлической кристаллической решетки гибче и пластичнее ионной, хотя внешне они весьма похожи. Отличительной особенностью ее является наличие положительно заряженных катионов (ионов метала) в узлах решетки. Между узлами живут электроны, участвующие в создании электрического поля, эти электроны еще называются электрическим газом. Наличие такой структуры металлической кристаллической решетки объясняет ее свойства: механическую прочность, тепло и электропроводность, плавкость.
Общее понятие о металлах
«Химия. 9 класс» – это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Читать также: Ключ разводной размеры по номерам
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.


Видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.


Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту [email protected] или в Фейсбук, с уважением автор.
Страница про автора
Эта статья доступна на английском – Crystal Lattice in Chemistry.
Атомно-кристаллическое строение металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку. Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение – это науки, которые занимаются изучением особенностей строения таких структур.
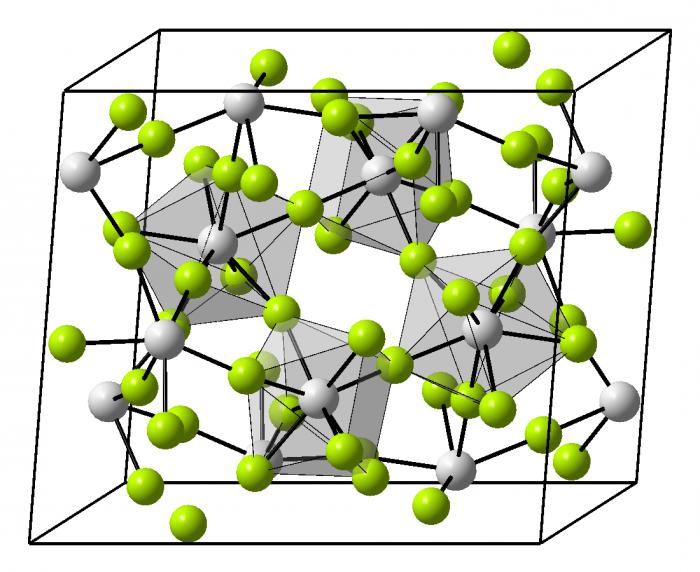

Сама элементарная ячейка – это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
Читать также: Пуансоны для гибки листового металла
Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность – в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.